树突状细胞(dendritic cell,DC)是目前发现的功能最强的抗原递呈细胞(APC),一个DC能够激活100-3000个T细胞,是巨噬细胞和B细胞的100-1000倍。DC通过处理肿瘤抗原并将其递呈给T细胞,能显著刺激初始T细胞增殖的APC,其他种类的APC(如巨噬细胞、B细胞)仅能刺激已活化或记忆T细胞。
目前DC体外培养主要是用细胞因子从骨髓、外周血和脐带血的DC前体定向诱导。骨髓和脐带血取样困难,外周血由于取材简单,不需要复杂的筛选和纯化过程,是目前临床获得DC的较好途径。
DC细胞治疗流程
-
细胞来源:患者外周血CD14+单核细胞、CD34+造血祖细胞; -
体外分化:使用GM-CSF和IL-4诱导CD14+单核分化为未成熟MoDC; -
抗原负载与成熟:负载肿瘤抗原如肿瘤特异性抗原肽(TSA)、肿瘤相关抗原(TAA)、肿瘤裂解物或预定抗原如蛋白或mRNA形式; -
诱导成熟:通过TNF-α+IL-1β+IL-6+PGE2因子组合诱导DC成熟; -
回输治疗:将成熟DC回输患者,可结合免疫检查点抑制剂(如PD-1)抗体增强疗效。
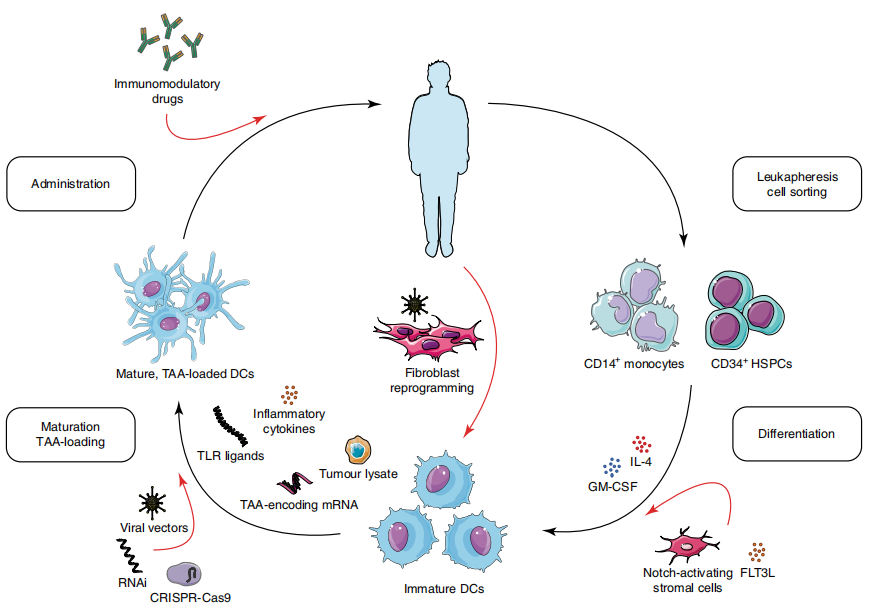
图1 :传统DC疫苗流程和新型优化策略示意图[1]
细胞因子的诱导机制
GM-CSF+IL-4:促进单核细胞向"大巨噬样细胞"分化;IL-4抑制DC前体向CD14+巨噬细胞分化,而分化为CD14-/CD1a-的iDC;
GM-CSF和IL4共同作用使单核细胞定向分化为iDC,此时的iDC具有较强的抗原摄取和加工能力,递呈能力很弱,细胞表面低中度表达MHCⅠ、Ⅱ类分子和B7家族分子(CD80、CD86等),但不表达或低表达CD14。
TNF-α+IL-1β:TNF-α激活NF-κB 信号通路,促进DC成熟(CD1a+/CD83+),IL-1β与TNF-α协同,强化DC成熟;TNF-α 和 IL-1β 主导 MHCⅡ类分子/共刺激分子表达
IL-6+PGE2:IL-6激活STAT3信号通路,PGE2是炎性介质,PGE2 和 IL-6可进一步提高DC的产量、成熟度、迁移能力和免疫激活能力,尤为重要的是DC迁移能力。
这一阶段mDC的抗原摄取和加工能力明显减弱,而抗原递呈能力显著增强,可极强地激活T细胞
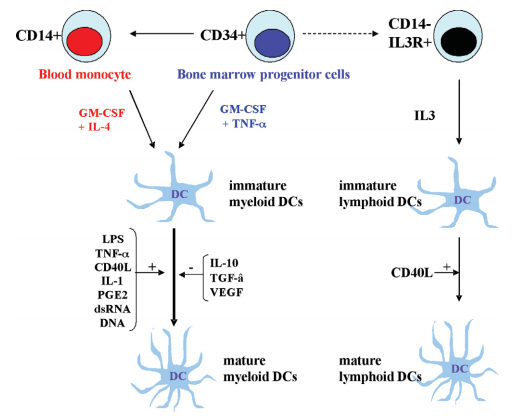
图2 :细胞因子诱导外周血CD14+单核细胞生成DC[2]
DC诱导培养实验流程[3,4,5,6]
01 外周血单核细胞收集
-
全血采集处理,Ficoll梯度离心法从全血中获得人外周血单个核细胞(PBMC);
-
贴壁法或磁珠法进行CD14+单核细胞富集。
贴壁法:2×106 cells/ml铺板PBMC,37℃培养1-2h使单核细胞贴壁,摇动培养板使非贴壁细胞松动并吸出
磁珠法:CD14+磁珠阳性分选,获得高纯度单核细胞
注意:PBMC中含有单核细胞和淋巴细胞,这一步目的是去除悬浮的淋巴细胞
02 DC细胞的培养
-
将单核细胞以1.5×106cells/ml密度铺至24孔板,加入含GM-CSF(100ng/ml)和IL4(50ng/ml)的完全培养基,培养箱培养2 天; -
第3天,进行半量换液,收集培养基到离心管,450g 4min离心,留上清,加入细胞培养板,再加入含GM-CSF和IL4的等体积新鲜培养基,培养箱培养2天;
注意:这一阶段贴壁的细胞会轻轻浮起来,是常见的半悬浮的DC。
-
第5天,轻轻吹打培养基,收获悬浮细胞和松散贴壁细胞,1000r 离心 5min,弃上清,收获未成熟的MoDC;
-
新鲜培养基重悬细胞,并加入TNF-α(10ng/ml)、IL-1β(10ng/ml)、IL-6(100ng/ml)和PEG2(1ug/ml),培养箱培养2-4天; -
第7-8天,多次吸液和排液松动贴壁不牢固的细胞,450g 4min离心收获成熟DC。
DC培养鉴定
01 形态学鉴定
5d后iDC细胞松散贴壁,外形不规则,有少许刺状突起,8d后典型是mDC,悬浮细胞增多,体积变大,大量细刺状突起。
02 流式细胞术
CD14(单核细胞特异性maker)、HLA-DR(人类白细胞抗原中的Ⅱ类分子)、CD1a/CD83(成熟DC特异性标志)、CD40/80/86(共刺激分子)、DC-SIGN(树突状细胞特异性细胞间黏附分子,参与捕获抗原)等分子的流式细胞检测方法通常用于分析树突状细胞的成熟状态及其功能特征。
03 细胞因子检测
人DC除了IL-6、TNF-α和MCP-1外,还常检测IL-12p70、IL-10和IL-1β,这些细胞因子更能全面反映人DC的免疫调节功能,小鼠DC检测的IL-6、TNF-α和MCP-1,更多反映其炎症反应和趋化能力。
04 混合淋巴反应(MLR)
MLR是基于DC能够激活T淋巴细胞引发免疫反应的原理,通过检测T细胞的增殖等反应来评估免疫应答强度。
近岸蛋白可提供DC体外诱导培养所需的科研级和GMP级细胞因子,高活性、低内毒素、高批间一致性,包含GM-CSF、IL-4、TNF-α、IL-6、IL-1β等,助力DC细胞的高效、稳定、合规培养。
高活性:细胞活性检测
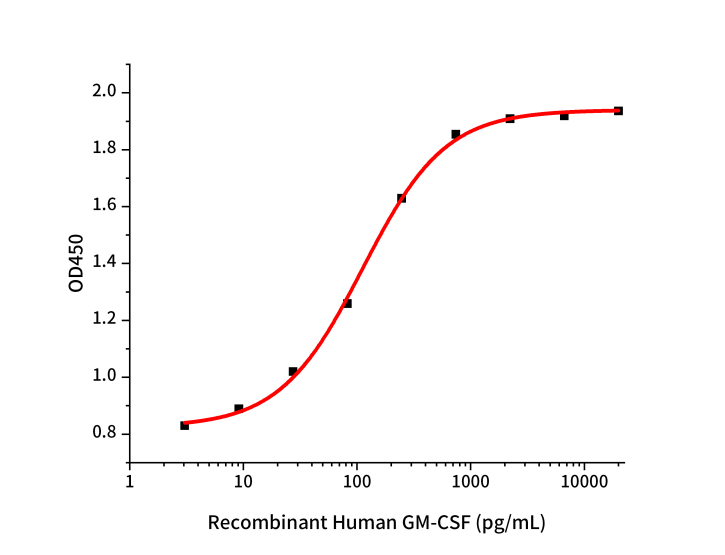
Measured in a cell proliferation assay using TF1 human erythroleukemic cells.The specific activity of recombinant human GM-CSF is ≥1.0 x 107 IU/mg, which is calibrated against the human GM-CSF Standard (NIBSC code: 88/646).
高批间一致性:确保实验可重复性
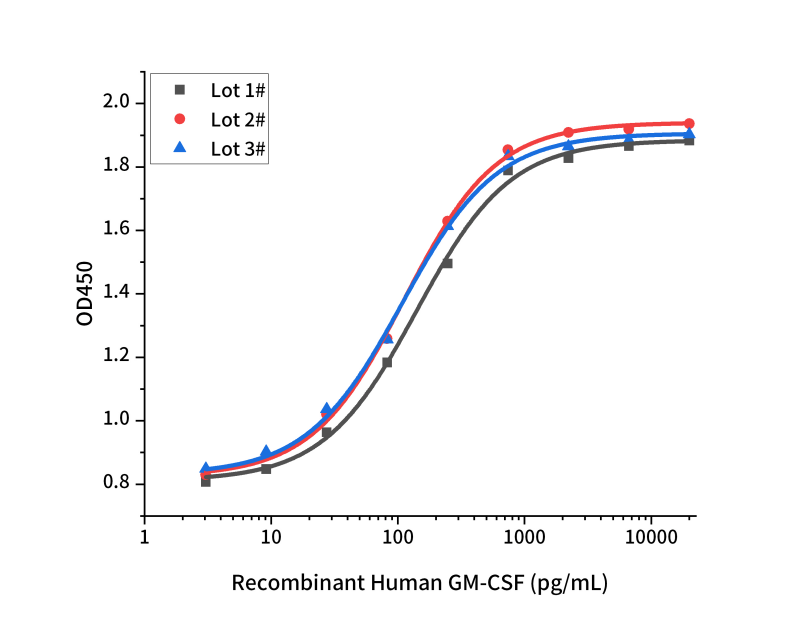
Measured in a cell proliferation assay using TF1 human erythroleukemic cells.The specific activity of recombinant human GM-CSF is ≥1.0 x 107IU/mg,Three independent lots were tested for activity and plotted on the same graph to show lot-to-lot consistency of GM-CSF.
DC培养相关产品
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
DC-CIK培养相关产品
|
|
|
|
|
|
|
DC 细胞生长扩增 |
|
|
|
CIK激活扩增 |
|
|
|
CIK 激活扩增,含 Anti-CD3、NovoNectin 等 |
|
|
|
CIK生长扩增 |
|
|
|
CIK生长扩增 |
参考文献
[1]Perez, Caleb R, and Michele De Palma. “Engineering dendritic cell vaccines to improve cancer immunotherapy.” Nature communications vol. 10,1 5408. 27 Nov. 2019, doi:10.1038/s41467-019-13368-
[2]Chung, N P-Y et al. “Dendritic cells: sentinels against pathogens.” Histology and histopathology vol. 19,1 (2004): 317-24. doi:10.14670/HH-19.317
[3]Jonuleit, H et al. “Pro-inflammatory cytokines and prostaglandins induce maturation of potent immunostimulatory dendritic cells under fetal calf serum-free conditions.” European journal of immunology vol. 27,12 (1997): 3135-42. doi:10.1002/eji.1830271209
[4]Gieseler, R et al. “In-vitro differentiation of mature dendritic cells from human blood monocytes.” Developmental immunology vol. 6,1-2 (1998): 25-39. doi:10.1155/1998/72054.
[5]陆小鹏,等. "人外周血单核细胞来源的树突状细胞的体外‘2+2’快速法培养及其鉴定." 动物学研究, vol. 29, no. 4, 2008, pp. 415-420. DOI:10.3724/SP.J.1141.2008.04415.
[6]Figueroa, Gloria et al. “Characterization of Human Monocyte-derived Dendritic Cells by Imaging Flow Cytometry: A Comparison between Two Monocyte Isolation Protocols.” Journal of visualized experiments : JoVE ,116 54296. 18 Oct. 2016, doi:10.3791/54296.
